- juillet 11, 2021
Prise en charge d’un patient porteur d’un dispositif électronique intracardiaque candidat à une radiothérapie
LES COLLABORATEURS

-
- Service de cardiologie, centre hospitalo-universitaire Hèdi Chaker, Sfax, Tunisie
- Service de radiothérapie oncologique, centre hospitalo-universitaire Habib Bourguiba, Sfax, Tunisie
- Service de carcinologie, centre hospitalo-universitaire Habib Bourguiba, Sfax, Tunisie
- Faculté de médecine, Sfax, Tunisie
I Objet
Gestion pré, per et post radiothérapie (RT) des patients porteurs d’un Dispositif Electronique Intra-Cardiaque (DEIC) : pacemaker (PM) ou défibrillateur automatique implantable (DAI)
II Application
III Contexte
Le nombre de patients, porteurs de DEIC et ayant un cancer justiciable d’un traitement par RT, est en perpétuelle croissance. Les DECI représentent une contre-indication relative à la RT d’où l’importance d’une mise en œuvre de mesures adaptées.
- 1. Quels sont les risques de la RT sur le bon fonctionnement des DEIC ?
-
- • Une dysfonction transitoire due à l’interférence électromagnétique (rare), responsable de « bruit » sur les différents canaux, pouvant entrainer une inhibition de la stimulation ou un traitement inapproprié de tachycardie (seulement sur les DAI). L’effet s’arrête avec l’arrêt de l’irradiation.
- • « Reset » en programmation « back-up » (fréquente) : le DEIC se programme en mode de secours, diffèrent selon les marques, la stimulation est assurée par un mode VVI (stimulation ventriculaire) avec sortie haute énergie, les traitements anti-tachycardies restent activés mais à des fréquences basses. Cette dysfonction qui n’est pas dose dépendante (effet stochastique) est le résultat d’un « conflit » dans l’algorithme du DEIC, et est certainement due à la production de neutrons par irradiation à haute énergie. Une reprogrammation manuelle est indispensable et permet généralement une récupération ad integrum des données du DEIC.
- • Dysfonction permanente (rare) : le plus souvent liée à la dose cumulée absorbée par le DEIC, généralement >5Gy. Elle nécessite un remplacement du matériel.
- 2. Quels sont les tumeurs dont le traitement par radiothérapie interfère avec le DEIC ?
Le traitement par radiothérapie peut interférer avec le DEIC pour les tumeurs de localisation thoracique, médiastinale ou cervicale basse : tumeurs mammaires, lymphomes non hodgkiniens médiastinaux, lymphomes de hodgkin cervico-médiastinaux, tumeurs pulmonaires, tumeurs cutanées et des parties molles de la région thoracique ou cervicale basse, tumeurs thymiques, tumeurs de l’œsophage cervico-thoracique, tumeurs de la région de la tête et du cou avec irradiation cervicale basse…
- 3. Quel type de rayonnement est impliqué dans le dysfonctionnement du DEIC au cours de la RT ?
Tout type de rayonnement produisant des neutrons peut être impliqué dans le dysfonctionnement du DEIC : les neutrons, les photons de haute énergie (>10MV), les protons et les ions lourds. NB :
-
- • L’irradiation des tumeurs de localisation thoracique ou médiastinale fait souvent appel à des photons de 6-10 MV
- • Le seuil pour une interaction neutrons-DEIC est de 0.6kev/µ
- • Les électrons ont peu d’interférences car ils produisent peu de neutrons : 5% (pour 15MeV) à 20% (pour 25MeV) de neutrons en dose équivalente par Gy pour des photons de même énergie.
- 4. Quelle dose et effet de débit de dose seuils sont à l’origine du dysfonctionnement du DEIC au cours de la RT ?
Tout La dose seuil qui peut entrainer des dommages au DEIC dépend du fabriquant et du modèle du dispositif : pour les nouveaux dispositifs certains dommages ont été observés même pour des doses ≤2Gy et pour d’autres l’effet est dit non stochastique (pas d’effet pour les faibles doses) ; mais, le risque de dysfonctionnement reste certain pour les doses modérées à élevées. Le débit de dose seuil recommandé est de 0.01gy/min (soit un DEIC placé à 5 cm de la bordure du champs ou à 2 cm dans le sens longitudinal du CBCT ou 4DCT FOV)
NB :-
- • Faire attention aux traitements hypo fractionnés (calcul d’équivalent de dose biologique).
- • Tenir compte de la dose cumulée par les différentes imageries embarquées MV.
- • Opter pour des champs de positionnement peu larges afin de réduire le diffusé de rayonnement.
- • Opter pour l’utilisation de dosimètres actifs in vivo afin de calculer la dose cumulée par le diffusé de rayonnement.
IV. Prise en charge
- 1. Précautions pré-radiothérapie
-
- • Identifier les patients porteurs de DEIC et informer le cardiologue/rythmologue
- • Déterminer la localisation tumorale
- • Évaluer le schéma de la RT, le type de rayonnement, l’emplacement du DEIC par rapport aux champs d’irradiation et la dose cumulée par le DEIC
- • Informer le patient des risques de la RT sur le DEIC
- • Récupérer la carte du patient ou le compte rendu d’implantation. Au minimum, il faut connaître la marque du PM/DAI, indispensable pour toute interrogation .
- • Organiser une évaluation cardiologique.
- • Le contrôle du DEIC est recommandé avant la RT. Les informations devant être communiquées par le rythmologue sont :
-
o Le type du DEIC
o La stimulo-dépendance définie par un rythme intrinsèque
o Nombre des sondes
o Site d’implantation
o Le mode programmé
o Les fréquences de stimulation minimale et maximale programmées
o Si l’asservissement est programmé ou non
o Le pourcentage de stimulation
o Les paramètres du dispositif sont-ils satisfaisants ? impédances, détection, seuil de stimulation
o La longévité de la batterie
o Si DAI, est ce qu’il y a eu des thérapies délivrées ? appropriées ou non ? et quand ?
- • La stratification du risque est faite selon : le type du DEIC (PM ou DAI), le caractère dépendant de la stimulation, une arythmie traitée récemment (pour les DAI), la dose maximale absorbée (<2 ou >5Gy) par le boitier, l’utilisation de photons à haute énergie

– La plupart des auteurs préconisent dans leurs protocoles la désactivation des thérapies ou l’utilisation d’un aimant systématique pour les défibrillateurs afin d’éviter les thérapies inappropriées.
– L’application d’un aimant est aussi recommandée chez les patients stimulodépendants (porteurs de PM)
- Appliquer et scotcher un aimant (Figure1) pendant toute la durée de la séance de RT chez ces patients
En effet, l’application d’aimant provoque :
– Pour le PM, une entrée en mode asynchrone à une fréquence magnétique variable selon les fabricants de 85 à 100/min, AOO, VOO, DOO selon la programmation initiale AAI, VVI ou DDD. Le PM est rendu « sourd » au bruit. Le retrait de l’aimant restaure la programmation initiale (mode synchrone).
– Pour le DAI, une inhibition intégrale pour tout modèle de DAI les thérapies anti- tachycardiques (stimulation anti-tachycardique et chocs internes), Par contre, le mode de stimulation habituelle est respecté. Le retrait de l’aimant restaure la programmation antérieure.
Les recommandations de l’HRS ( Heart Rhythm Society ) 2017 s’accordent pour souligner le caractère à risque d’une intervention prophylactique de remplacement de boitier en dehors du champ qui nécessiterait une réimplantation des sondes voire l’extraction des anciennes sondes. Le repositionnement de boitier est incontournable s’il ne permet pas un traitement de radiothérapie optimal sur la tumeur. Les recommandations américaines préconisent de ne pas dépasser une dose absorbée de 5Gy sur le boitier. La décision de déplacement du DEIC doit être prise après discussion avec le patient, la cardiologue, le rythmologue, l’oncologue et le radiothérapeute.
- 2. Précautions per-radiothérapie
-
- • La prise en charge au cours du traitement dépend de la stratification du risque
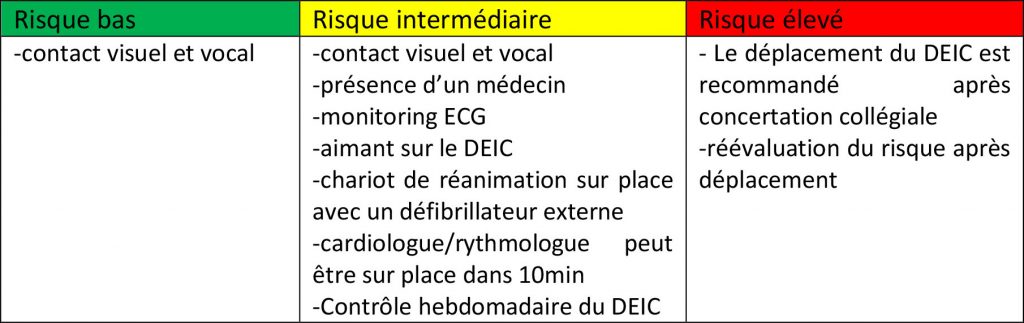
- 3. Précautions post-radiothérapie
-
- • Le suivi rythmologique dépend du risque de dysfonctionnement du DEIC.
- • Il est conseillé de faire un suivi rythmologique à la fin du traitement par radiothérapie, 1, 3 et à 6 mois de la fin de radiothérapie
1.Indik JH et al. 2017 HRS expert consensus statement on magnetic resonance imaging and radiation exposure in patients with cardiovascular implantable electronic devices. Heart Rhythm. 2017
2. Zaremba T, et al. Radiotherapy in patients with pacemakers and implantable cardioverter defibrillators: a literature review. Europace. avr 2016;18(4):479-91.
3. Gauter-Fleckenstein B et al. Strahlenther Onkol Organ Dtsch RontgengesellschaftAl 2015
4. Barillot I et al. Cancer Radiother2016.
5. A Huertas et al. Management of patients with pacemakers or implantable cardioverter defibrillator undergoing radiotherapy. Cancer Radiother (2018)
6. Benjamin Gauter-Fleckenstein et al. DEGRO/DGK guideline for radiotherapy in patients with cardiac implantable electronic devices. Strahlenther Onkol 2015.
7. Ardalan Sharifzadehgan et al. Radiotherapy in Patients with a Cardiac Implantable Electronic Device. The American Journal of Cardiology 2020