- mars 5, 2021
Prise en charge de la maladie thromboembolique veineuse chez les patients atteints de cancer
LES COLLABORATEURS
-
- Service de cardiologie, centre hospitalo-universitaire Hèdi Chaker, Sfax, Tunisie
- Service de carcinologie, centre hospitalo-universitaire Habib Bourguiba, Sfax, Tunisie
- Service de radiothérapie oncologique, centre hospitalo-universitaire Habib Bourguiba, Sfax, Tunisie
- Faculté de médecine, Sfax, Tunisie
I Objet
II Application
III Contexte
IV Prise en charge
- 1. Traitement curatif de la MTEV
- Chez les patients avec clairance de la créatinine ≥30 ml/min :
-
- -Utiliser de préférence une HBPM ou un AOD.
- -Deux schémas thérapeutiques sont possibles :
-
-HBPM dose curative pendant au moins 6 mois
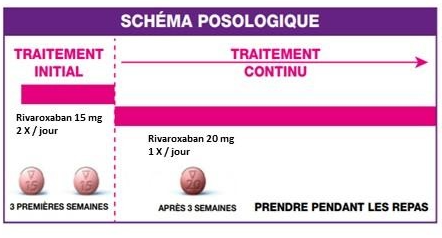
En cas d’impossibilité de continuer les HBPM dose curative pendant 6 mois, un switch par AVK est discutable. -AOD pendant 6 mois-Rivaroxaban dès J1 à la dose de 15 mg X2/ jour pendant les trois premières semaines. Après ce traitement initial, la posologie sera de 20 mg / jour.
-
-
-Ou Edoxaban (molécule non encore disponible en Tunisie) après 5 jours d’anticoagulation parentérale)
-
-Les AOD sont à utiliser :
-
-En l’absence de risque élevé d’hémorragie gastro-intestinale ou génito-urinaire
-
-En l’absence d’interaction médicamenteuse ou d’altération de l’absorption gastro-intestinale.
-
-Avec prudence en cas de cancer digestif, en particulier en cas de tumeur du tractus digestif supérieur, compte tenu du risque élevé de de saignement observé avec l’Edoxaban et la Rivaroxaban.
-
- Chez les patients avec clairance de la créatinine <30 ml/min :
-
-L’HNF et la Fondaparinux sont préférés aux HBPM.
-
-Les HBPM doivent être utilisés à doses adaptées avec surveillance de l’activité́ anti-Xa
- – La thrombolyse en cas d’EP grave (avec état de choc) est à discuter au cas par cas avec une attention extrême aux contre-indications, notamment en cas de risque hémorragique (métastase cérébrale).
- – La pose de filtre cave peut être envisagée dans le traitement initial en cas de contre-indication aux anticoagulants ou de récidive d’EP malgré un traitement anticoagulant optimal. Une réévaluation périodique des contre-indications est recommandée, et les anticoagulants doivent être repris dès que leur utilisation est sans danger.
-
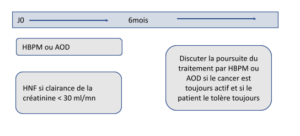
- – Au moins 6 mois à poursuivre tant que le cancer est actif ou traité
- – Après 6 mois de traitement, la décision de poursuivre ou d’arrêter les anticoagulants (AOD, AVK ou HBPM) doit être basée sur une évaluation individuelle du rapport bénéfice / risque, de la tolérance, de la préférence des patients et de l’activité tumoral.
- – Indication à un traitement par HBPM pour une durée de 3 mois.
- – Le cathéter central peut être laissé en place s’il est fonctionnel, bien positionné, non infecté et si l’évolution des symptômes est favorable sous traitement anticoagulant
- 2. Traitement préventif de la MTEV
- – HBPM à dose préventive en 1 injection sous cutanée par jour ou calciparine en 3 injections sous cutanée/ jour.
- – Il n’existe aucune donnée justifiant l’emploi du fondaparinux comme alternative aux HBPM pour la prévention primaire de la MTEV post opératoire chez les patients atteints de cancer devant subir une intervention chirurgicale
- – La thromboprophylaxie doit être débutée 12 à 24 heures avant l’intervention et poursuivie au moins 7 à 10 jours.
- – Une prophylaxie prolongée (4 semaines) est indiquée après chirurgie majeure par laparotomie ou laparoscopie chez les patients à haut risque de MTEV (cancer du pancréas, cancer métastatique, ou score de Khorana ≥3) et à faible risque hémorragique.
- – La pose de filtre cave n’est pas recommandée.
- – Patients atteints de cancer hospitalisés et à mobilité réduite: prophylaxie par HBPM, calciparine ou fondaparinux (molécule non encore disponible en Tunisie)
- – Patients avec un cancer à haut risque de MTEV (cancer du pancréas localement avancé, cancer métastatique, ou score de Khorana ≥3) et faible risque hémorragique : HBPM
- – Patients ambulatoires traités par chimiothérapie systémique à risque intermédiaire ou élevé de MTEV (cancer du pancréas ou score de Khorana ≥2), en l’absence de saignement actif et en l’absence de risque hémorragique élevé :
-
– AOD (Rivaroxaban 10 mg/j (disponible en Tunisie) ou Apixaban 2,5 mg X 2 /j
(molécule non encore disponible en Tunisie)) – Faire attention aux CI des AOD
-
- – Chez les patients ambulatoires traités par chimiothérapie systémique, une prophylaxie pharmacologique systématique par HBPM, AVK ou AOD n’est pas recommandée si le risque de MTEV est faible
- – La thrombo-prophylaxie primaire par HBPM n’est pas indiquée chez les patients en ambulatoires atteints de cancer du poumon localement avancé ou métastatique traités par chimiothérapie systémique, y compris ceux ayant un faible risque hémorragique.
- – Chez les patients atteints de myélome multiple et traités par Immuno-modulateurs + corticoïdes et/ou chimiothérapie : une prophylaxie de la MTEV est recommandée :
– Les HBPM à dose préventive sont recommandés
– Certaines études ont montré des effets similaires en termes de thrombo-prophylaxie primaire avec de faibles doses d’aspirine
- 3. Situations particulières
- 3.1.1. En cas de traitement curatif de la MTEV
- – Taux de plaquettes >50 000 éléments/mm3 sans signes hémorragiques : HBPM à doses curatives
- – Taux de plaquettes <50 000 éléments/mm3 ⇒ Discussion collégiale (évaluation du rapport bénéfice/risque).
- 3.1.2. En cas de traitement préventif de la MTEV
- – Taux de plaquettes > 80 000 éléments/mm3 sans signes hémorragiques : HBPM à doses préventives
- – Taux de plaquettes <80 000 éléments/mm3 ⇒ Discussion collégiale (évaluation du rapport bénéfice/risque)
- – Les HBPM ou les AOD sont indiqués pour le traitement curatif de la MTEV.
- – Chez les patients atteints de tumeur cérébrale devant subir une intervention neurochirurgicale, une thrombo-prophylaxie primaire par HBPM ou HNF, débutée en post opératoire, est recommandée.
- – La thrombprophylaxie primaire chez les patients atteints d’une tumeur cérébrale qui ne vont pas subir une intervention neurochirurgicale n’est pas recommandée.
- – HBPM pour le traitement curatif de la MTEV
- – HBPM pour le traitement préventif de la MTEV
- – Les AVK et les AOD sont à éviter
- – Patient sous HBPM ⇒ ➚ la dose d’HBPM de 20-25%
- – Patient sous AOD ⇒ switcher vers HBPM
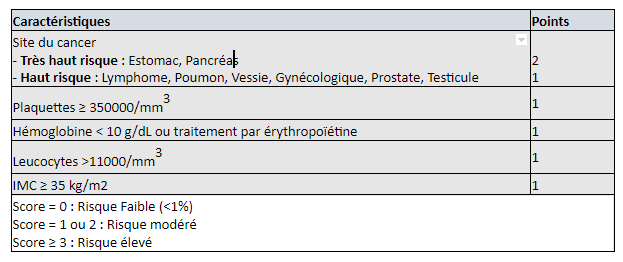 Annexe 1 : Score de Khorana : Score qui permet d’évaluer le risque de MTEV des patients avec cancer stade avancé avant la chimiothérapie
Annexe 1 : Score de Khorana : Score qui permet d’évaluer le risque de MTEV des patients avec cancer stade avancé avant la chimiothérapie1. Farge D, Frere C, Connors JM, Ay C, Khorana AA, Munoz A, et al. 2019 international clinical practice guidelines for the treatment and prophylaxis of venous thromboembolism in patients with cancer. The Lancet Oncology. 2019;20(10):e566‑81. 2. Debourdeau P, Cossou-Gbeto C, Takam-Sohwe T, Laroche J-P. Low-molecular-weight heparins for cancer-associated thromboembolism: What place in 2019? Bulletin du Cancer. 2020;107(2):224‑33.